冠動脈の血行動態モデル
末端樹木モデルに基づいたヘッドロスありの0Dモデル
(A patient-specific lumped-parameter model of coronary circulation / Zheng Duanmu)
モデル化
冠動脈全体の類似回路網を図7 に示す。 この回路網では、冠動脈のすべての端末が、構造化樹木モデルから計算されたルート・インピーダンスに割り当てられている。Pietrabissaらによる研究7 と同様に、このネットワークには心血管系の閉ループモデルが含まれています。心筋内圧(RVPG および LVPG 時)は圧力発生器として機能し、心臓内の冠動脈の位置に応じて、心室内圧の 3 分の 1 または半分に選ばれる26。冠動脈はモデル内でシミュレートされ、同時に右心房にリンクされる。また、全身循環と肺循環も含まれている。右心室圧発生装置(RVPG)と左心室圧発生装置(LVPG)はフィードバック項である。左冠状静脈(LCV)と右冠状静脈(RCV)もターミナルインピーダンス(Z)としてシステムに接続される。

冠動脈樹は閉ループの循環器系で表現し、R hは 頭部損失による変動抵抗、Z1~Z10は冠動脈血管の末端に取り付けた構造化樹モデルのルートインピーダンスである。
集中定数モデルの数理
血液をニュートン流体とし、血管を円筒管とする。各血管内の流れの支配方程式は
ここで、pは圧力、Δp は圧力損失、qは流量である。その他のパラメータは、水力抵抗R、各血管の弾性容量C、血流の慣性Lである。したがって、回路における抵抗、静電容量、インダクタンスに類似して、以下のようになる
ここで,μは血液粘度,ρは密度,Gは血管のヤング率,lはセグメント長,Dは直径,hは血管の肉厚である.CTデータから推定した全血管のパラメータを表1に示す。心拍数は75回/分(心周期0.8秒)で計測した。また、
とし、Dを血管径として壁厚hは 0.08D とした
CTデータから推定された患者別冠動脈モデルのパラメータ

血液は心室から供給されるため、左心室(LV)と右心室(RV)のポンプ機能を以下のように選択した。
ここで、P v は心室圧、U0は体積V0でのピーク等体積圧、Eは時間変化するエラスタンス、活性化関数σ(t) = [1 -cos(2πt/t s) ]である。t s は収縮期、Vは基準容積、𝑉 ˙ V˙ は容積変化率、 R v は心室心筋の抵抗、E d はパッシブエラスタンスである。

血管分岐部でのインピーダンスは
N世代からなる対称木の端子インピーダンスは

動脈漸減指数率を2.76としたときの娘血管rd、親血管rpの比α=rd/rp = 0.778
r0は元のルート半径
λ = 50は小動脈の長さと半径の比を定義する定数
ヘッドロスの評価
血管構造に伴うエネルギー損失と損失係数は、ベルヌーイの式に組み込むことができる9。図8に示すような冠動脈の入口部におけるヘッドロス(断面積変化による急激な圧力損失)をモデル化するために、圧力損失を次のように推定する。
ξは局所抵抗であり,血管狭窄径比 0.5,Re=100 の場合,Festerらの経験式 ξ=288/Re から 2.88 と推定され,vは平均流速である.そして、ヘッドロスによる抵抗R hは
上記を計算すると、冠動脈の半径r(mm)を用いて、

左右の冠動脈樹のヘッドロスの位置と、断面積の狭窄によるヘッドロスの位置。
冠動脈の1Dモデル
A One-Dimensional Hemodynamic Model of the Coronary Arterial Tree (Zheng Duanmu1)
冠動脈末端のモデリング


べき乗則
各末端大動脈の遠位端は,心筋内にある小血管の血管床(モデルでは構造化ツリーで表現)に接続されている.構造化木では、半径rpの親血管は半径rd1=αrpとrd2=βrpの2本の子血管に分岐する(0<β<α<1)。分岐過程は以下。ξは半径指数、ηは面積比、γは非対称比。ξ = 2.76

1D冠動脈のモデリング
連続の式と運動量方程式
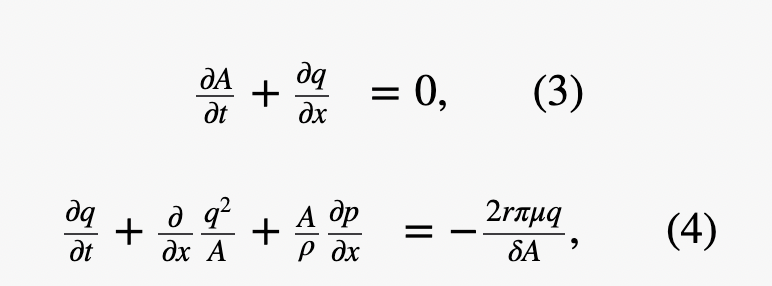
血管の流体力学
Numerical Simulation and Experimental Validation of Blood Flow in Arteries with Structured-Tree Outflow Conditions, OLUFSEN
大血管における流体力学
血管の典型的な流体力学的モデリングの仮定は以下
- 不透過性
- 軸対称
- 弾性円筒
- 非圧縮性(密度ρは一定)
- ニュートン流体(粘性μは一定)
- 流体の圧力P(x,t)は面積に依存しない(rに依存しない)
- 血管は指数関数的に先細りになる
- 血管は半径方向のみに動き、軸方向には動かない
- 血管内膜に接する場所での軸方向速度は0
連続の式
上記を断面積で積分して、
以上より、断面積Aと流量qを用いて、
運動量保存
連続の式を使い変形を進めると
境界層近似を行い、下記のような流速曲面を仮定する
上記を用いて計算すると、
以上より一次元の運動方程式は
これは解析的に解けないため、2段階Lax–Wendroff法を用いた数値計算を行う。
保存則形式にする
また、下記のようにBを導入すると、
以上より下記の保存則形式を得る。
血管内壁条件・ラプラスの法則
ここで、
小血管
分岐部境界条件
質量保存
エネルギー保存
ベルヌーイの定理。エネルギー損失は親速度の2乗に比例(比例定数K)
速度はすべて平均速度
ただし、細動脈では下記の式のように圧保存で近似できる。
流出路境界条件
小動脈は二元的かつ非対称的に構造化された木の集合体。
そのような木はそれぞれ、細動脈のレベルに達するまでの世代数が可変。
なぜなら、そのレベルが大動脈と細動脈をつなぐ小動脈では、粘性効果が大動脈よりも重要であり、慣性効果はそれに比例して小さくなる。大動脈と細動脈をつなぐ小動脈では、粘性効果が大動脈よりも重要であり、慣性効果はそれに比例して小さくなる。従って、非線形項は削除し、粘性効果をより詳細にモデル化する。
また、各血管を直線として扱うことである。特に、小動脈の各樹木の根元のインピーダンスを再帰的な数値手順で計算することができる。これらのルートインピーダンスは、大動脈の流出境界条件となる
小血管での流体力学方程式
大血管のナビエ・ストークス方程式と比較して、慣性項が粘性項より小さいため、これを無視すると、
各種パラメータ

In vivo Coronary flow

(https://journals.physiology.org/doi/full/10.1152/ajpheart.00603.2013 より)
収縮早期(S1)、収縮後期(S2)、拡張早期(D1)、拡張後期(D2)
冠動脈狭窄のモデル化
α = AS/A0
A0: 正常断面積, AS: 狭窄した面積
α = 100 − p, p: 面積減少率

PDAの狭窄の程度が異なる場合の圧力(左)と流量(右)。

(a)冠動脈の狭窄とFFRの典型的な表示。(b)シミュレーションのPDA対狭窄部、Pijls & Bruyneによる測定との比較、(c)無次元流体シミュレーション対狭窄部、Matesらによる測定との比較.
冠動脈の0Dモデルでどのように患者データから推定するか
冠動脈の長さと冠動脈体積のスケーリング関係を使う方法
Estimation of the flow resistances exerted in coronary arteries using a vessel length-based method(Kyung Eun Lee)


心筋の血管の構造と密度が似ていることから,すべての抵抗がほぼ同じであり,共通の値(R 1 = R 2= ...= R n)で 表されると仮定する
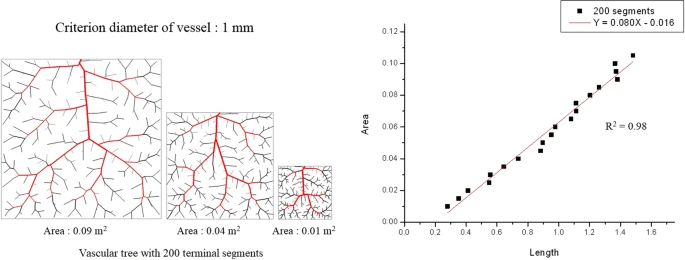
ここで、nは娘血管の分岐密度に直接関係する。図1に示すように、娘血管は母血管に沿ってほぼ一様に分布しているため、娘血管の数nは母血管の長さlに比例する
LV体積はRV体積の3.46倍であるという臨床観察
様々な面積(0.09 m2, 0.04 m2, 0.01 m2など)で最適化した血管フラクタル木のモデリング(左図)と、面積(体積)と血管の全長との直線関係(右図)。



参考文献
- Analysis of lumped parameter models for blood flow simulations and their relation with 1D models
血管網の0次元モデルが1次元の線形システムの1次離散化と見なすことができることを証明 - Mathematical analysis of the quasilinear effects in a hyperbolic model blood flow through compliant axi-symmetric vessels
Navier-Stokes方程式の軸対称形式の特性を詳細に研究している。血管の半径が特性波長に対して小さい場合、半径方向の運動量方程式は、圧力がどの断面でも一定であることを示し、血管の断面積で軸方向に運動量方程式を積分すると、半径方向の速度項は面積項に包含されることを実証した。この仮定は実用的な血管の流れに対して有効であるため、結果として得られる1次元モデルは、流れ、圧力、面積を基本変数として定式化することの妥当性を与える - Review of Zero-D and 1-D Models of Blood Flow in the Cardiovascular System
包括的なレビュー

Discussion